31/07/2013 - 21:35
Đình chỉ lưu hành thuốc Phil Bone-Care, rút số đăng ký thuốc Relab
-
700 thầy thuốc tham dự Hội nghị khoa học nhi khoa khu vực ĐBSCL mở rộng lần X năm 2026

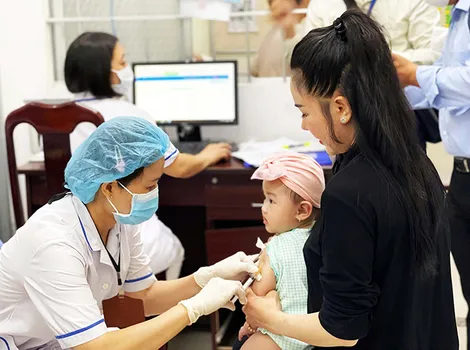
- Trẻ dưới 6 tuổi được khám sức khỏe miễn phí ít nhất 1 lần/năm
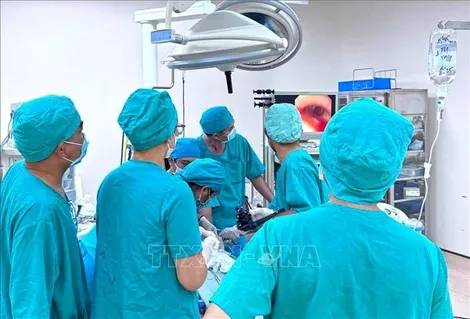
- Bệnh viện Đa khoa Trung ương Cần Thơ thực hiện thành công 20 ca ghép thận trong 2 năm
- Ngày Thalassemia thế giới (8-5): Sàng lọc bệnh, tật bẩm sinh: Chìa khóa bảo vệ thế hệ tương lai
- Tăng huyết áp - “Kẻ” gây tử vong thầm lặng
- Phòng ngừa bệnh mãn tính - “chìa khóa” sống lâu và khỏe mạnh
- Nâng chất toàn diện mạng lưới y tế cơ sở trong giai đoạn mới
- Nguy cơ của COVID-19 đối với bệnh nhân mắc bệnh phổi tắc nghẽn mạn tính
- Sỏi ống mật chủ - Nguy hiểm âm thầm, điều trị hiệu quả nhờ kỹ thuật chuyên sâu
- Mỗi người dân được khám sức khỏe miễn phí 1 lần/năm
-
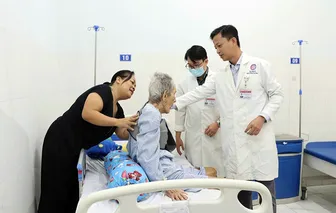
Cụ ông gần 100 tuổi phẫu thuật thay khớp háng thành công tại Bệnh viện Trường Đại học Y Dược Cần Thơ
- Cần Thơ: Nâng cao năng lực quản lý điều dưỡng qua các mô hình cải tiến
- Không chủ quan khi bà bầu bị tăng huyết áp
- Phòng ngừa mất nước và rối loạn điện giải cho thai phụ trong những ngày nắng nóng
- Sở Y tế TP Cần Thơ ký kết hợp tác cùng Hệ thống Y tế MEDLATEC
- TP Cần Thơ khen thưởng đột xuất Bệnh viện Đa khoa thành phố về ca ghép thận đầu tiên thành công
- Thiên Môn Bổ Phổi hỗ trợ người hay ho do viêm họng, viêm phế quản
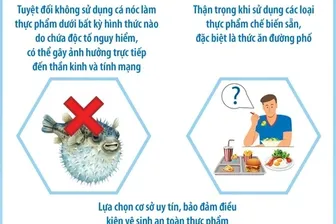
- Lưu ý an toàn thực phẩm mùa nắng nóng
- Điều trị đục thủy tinh thể bằng công nghệ phaco không dao tại Cần Thơ
- Đi bộ 10.000 bước/ngày giảm nguy cơ mắc bệnh và tử vong do ngồi nhiều